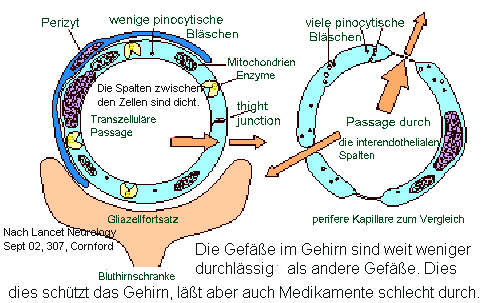
 engl. blood-brain barrier) diese schützt das Gehirn vor Giften und anderen potentiell schädlichen Substanzen. Es ist also eine Art spezieller Schutzschild des Gehirns. Viele Substanzen, wie Hormone oder Transmitter, die im Blut zirkulieren Katecholamine, Glutamat haben auch eine Transmitterfunktion im Gehirn, müssen dort aber für die Funktion zu anderen Zeitpunkten und in anderen Mengen ausgeschüttet werden. Serotoninbestimmungen im Blut sind deshalb beispielsweise nicht aussagekräftig für einen Mangel im Gehirn. Ebensolches gilt für das Ionenmillieu. Viele Gifte werden durch die Bluthirnschranke dem Hirn ferngehalten. Die hirneigenen Endothelzellen erwerben ihre Barriereeigenschaften in der Wechselbeziehung mit dem neuroektodermalen Mikromilieu und verlieren sie unter pathologischen Bedingungen. Während der embryonalen Entwicklung werden die Endothelzellen auf den Blut-Hirn-Schranken-Phänotyp geprägt, wobei wahrscheinlich transiente Cadherin-vermittelte Kontakte mit Perizyten eine wichtige Rolle spielen. Struktur und Funktion von Adherens und Tight Junctions der Blut-Hirn Schranke werden im Rahmen der Angiogenese durch Wachstumsfaktoren moduliert. Die Kapillaren (kleinste haardünne Blutgefäße) des Gehirns sind anders gebaut als im übrigen Körper. Eine dichte Plasmamembran zwischen den Zellen verhindert im Gegensatz zu den peripheren Zellen das Durchdringen durch Gifte und viele andere Substanzen. Insbesondere große Moleküle werden nicht durchgelassen. Die Bluthirnschranke verfügt allerdings über spezielle Transportmechanismen. Es gibt spezielle Transport- und Rezeptorproteine an der Bluthirnsschranke. Allerdings können dadurch auch Medikamente, Gene, und andere therapeutisch und diagnostisch genutzte Substanzen schlechter zum Gehirn eindringen. Für viele moderne Therapien ist gerade das gezielte Erreichen des betroffenen Organs oder der kranken Zellen der wichtigste Aspekt der über die Wirksamkeit entscheidet. Medikamente gegen Hirntumoren sollen nur den Tumor schädigen und die gesunden Stellen schonen. Sie sollen damit auch überwiegend am Tumor die Bluthirnschranke überwinden. Psychopharmaka sollen im Gehirn konzentriert werden und in der Peripherie wenig Nebenwirkungen verursachen. Teilweise sind solche Ansätze gelungen. Geforscht wird derzeit an Substanzen, die sie an Moleküle anlagern, die speziell von der Bluthirnschranke aufgenommen werden, oder auch an Antikörpern gegen Rezeptoren, die speziell gegen die endothelialen Zellen im Gehirn gerichtet sind um so den Transport dieser Medikamente durch die Bluthirnsschranke zu ermöglichen. Dies mit Chancen und entsprechenden Risiken. Die Durchlässigkeit der Bluthirnschranke für bestimmte Toxine, Medikamente oder Xenoproteine ist u.a. genetisch festgelegt. Die Expression des Choroidplexus Epithels für das MDR1 P Glykoprotein und das Multidrug- Resistance-associated Protein scheinen ein Rolle bei der Durchlässigkeit der Bluthirnschranke für Medikamente zu spielen. Eine Veränderung der Durchlässigkeit der Blut-Hirn-Schranke kann zum Hirnödem führen. Verschiedene Erkrankungen wie Tumore, Traumata, Ischämien, Meningoenzephalitis, Multiple Sklerose und diabetische Stoffwechselstörungen führen umgekehrt zu einer vermehrten Durchlässigkeit der Bluthirnschranke. Eine abnorme Durchlässigkeit der Bluthirnschranke könnte auch für verschiedene Erkrankungen ursächlich sein. Beispielsweise wird eine solche Ursache für lakunäre Hirninfarkte, Leukoaraiosis, und Demenz postuliert . Dies könnte auch der Grund sein, warum Diabetiker besonders anfällig für die genannten Erkrankungen sind.
engl. blood-brain barrier) diese schützt das Gehirn vor Giften und anderen potentiell schädlichen Substanzen. Es ist also eine Art spezieller Schutzschild des Gehirns. Viele Substanzen, wie Hormone oder Transmitter, die im Blut zirkulieren Katecholamine, Glutamat haben auch eine Transmitterfunktion im Gehirn, müssen dort aber für die Funktion zu anderen Zeitpunkten und in anderen Mengen ausgeschüttet werden. Serotoninbestimmungen im Blut sind deshalb beispielsweise nicht aussagekräftig für einen Mangel im Gehirn. Ebensolches gilt für das Ionenmillieu. Viele Gifte werden durch die Bluthirnschranke dem Hirn ferngehalten. Die hirneigenen Endothelzellen erwerben ihre Barriereeigenschaften in der Wechselbeziehung mit dem neuroektodermalen Mikromilieu und verlieren sie unter pathologischen Bedingungen. Während der embryonalen Entwicklung werden die Endothelzellen auf den Blut-Hirn-Schranken-Phänotyp geprägt, wobei wahrscheinlich transiente Cadherin-vermittelte Kontakte mit Perizyten eine wichtige Rolle spielen. Struktur und Funktion von Adherens und Tight Junctions der Blut-Hirn Schranke werden im Rahmen der Angiogenese durch Wachstumsfaktoren moduliert. Die Kapillaren (kleinste haardünne Blutgefäße) des Gehirns sind anders gebaut als im übrigen Körper. Eine dichte Plasmamembran zwischen den Zellen verhindert im Gegensatz zu den peripheren Zellen das Durchdringen durch Gifte und viele andere Substanzen. Insbesondere große Moleküle werden nicht durchgelassen. Die Bluthirnschranke verfügt allerdings über spezielle Transportmechanismen. Es gibt spezielle Transport- und Rezeptorproteine an der Bluthirnsschranke. Allerdings können dadurch auch Medikamente, Gene, und andere therapeutisch und diagnostisch genutzte Substanzen schlechter zum Gehirn eindringen. Für viele moderne Therapien ist gerade das gezielte Erreichen des betroffenen Organs oder der kranken Zellen der wichtigste Aspekt der über die Wirksamkeit entscheidet. Medikamente gegen Hirntumoren sollen nur den Tumor schädigen und die gesunden Stellen schonen. Sie sollen damit auch überwiegend am Tumor die Bluthirnschranke überwinden. Psychopharmaka sollen im Gehirn konzentriert werden und in der Peripherie wenig Nebenwirkungen verursachen. Teilweise sind solche Ansätze gelungen. Geforscht wird derzeit an Substanzen, die sie an Moleküle anlagern, die speziell von der Bluthirnschranke aufgenommen werden, oder auch an Antikörpern gegen Rezeptoren, die speziell gegen die endothelialen Zellen im Gehirn gerichtet sind um so den Transport dieser Medikamente durch die Bluthirnsschranke zu ermöglichen. Dies mit Chancen und entsprechenden Risiken. Die Durchlässigkeit der Bluthirnschranke für bestimmte Toxine, Medikamente oder Xenoproteine ist u.a. genetisch festgelegt. Die Expression des Choroidplexus Epithels für das MDR1 P Glykoprotein und das Multidrug- Resistance-associated Protein scheinen ein Rolle bei der Durchlässigkeit der Bluthirnschranke für Medikamente zu spielen. Eine Veränderung der Durchlässigkeit der Blut-Hirn-Schranke kann zum Hirnödem führen. Verschiedene Erkrankungen wie Tumore, Traumata, Ischämien, Meningoenzephalitis, Multiple Sklerose und diabetische Stoffwechselstörungen führen umgekehrt zu einer vermehrten Durchlässigkeit der Bluthirnschranke. Eine abnorme Durchlässigkeit der Bluthirnschranke könnte auch für verschiedene Erkrankungen ursächlich sein. Beispielsweise wird eine solche Ursache für lakunäre Hirninfarkte, Leukoaraiosis, und Demenz postuliert . Dies könnte auch der Grund sein, warum Diabetiker besonders anfällig für die genannten Erkrankungen sind.
Quellen / Literatur:
Lancet Neurology 2002; 1: 306-15, NWG 4/00, PNAS Vol. 96, 3900-3905, 1999, J.M. Wardlaw, P.A.G. Sandercock, M.S. Dennis, J. Starr, and H. Kalimo Is Breakdown of the Blood-Brain Barrier Responsible for Lacunar Stroke, Leukoaraiosis, and Dementia? Stroke, March 1, 2003; 34(3): 806 – 812. [Abstract] J M Starr, J Wardlaw, K Ferguson, A MacLullich, I J Deary, and I Marshall, Increased blood-brain barrier permeability in type II diabetes demonstrated by gadolinium magnetic resonance imaging J. Neurol. Neurosurg. Psychiatry, January 1, 2003; 74(1): 70 – 76. [Abstract]

